ELISAs und Schnelltests
vWF-PP ELISA
ELISA zur quant. Messung des von-Willebrand-Faktor-Propeptids (vWF-PP)
Der Von-Willebrand-Faktor (VWF) hat mehrere wichtige Funktionen in der primären Hämostase. Das multimere Protein findet sich im Plasma, in Thrombozyten und Endothelzellen. VWF ist auch ein Trägerprotein und Stabilisator für den Gerinnungsfaktor VIII (FVIII) im Plasma.
Während der Biosynthese von VWF-Multimeren wird ein 100 kDa großes Glykoprotein-Propeptid (VWF:PP) proteolytisch gespalten und im Plasma freigesetzt. Bei bestimmten Arten von VWF-Erkrankungen, darunter erbliche oder erworbene Formen, Mutationen und einige andere Krankheiten, können abnormale Konzentrationen sowohl von VWF:PP als auch von VWF:AG (VWF Antigen) oder VWF-Aktivität festgestellt werden, was sich im Verhältnis von VWF:PP und VWF:AG zeigt.
Menschen mit einer VWF-Erkrankung zeigen eine erhöhte Blutungsneigung, z. B. Epistaxis, Zahnfleischbluten, Hämatome oder übermäßige Blutungen nach zahnärztlichen oder anderen chirurgischen Eingriffen. In extremen Fällen eines absoluten Mangels (VWF-Krankheit Typ 3) kann es zu lebensbedrohlichen Blutungen kommen. Im Blut weisen VWF und VWF:PP sehr unterschiedliche Halbwertszeiten auf (12 versus 2 Stunden). Die Messung von VWF:PP ist neben VWF:AG ein wichtiges Instrument zur Charakterisierung der Art des VWF-Mangels, insbesondere bei Personen mit einer verkürzten Plasmahalbwertszeit von VWF.
Die Kavitäten der in diesem Kit enthaltenen Mikrotiterplattenstreifen sind mit einem gegen VWF:PP gerichteten monoklonalen Antikörper beschichtet. Die Probe wird in eine Kavität pipettiert, gefolgt von einem zweiten monoklonalen Antikörper gegen VWF:PP, der mit einem Enzym konjugiert ist. VWF:PP bindet an den Antikörper, der an die feste Phase gebunden ist, und wird immobilisiert.
Der zweite Antikörper mit dem konjugierten Enzym bindet ebenfalls an den immobilisierten VWF:PP. Nach der Inkubation und den Waschschritten wird alles ungebundene Material entfernt, und das zugegebene Substrat wird durch das gebundene Enzym des Konjugats gespalten und setzt einen Farbstoff im Verhältnis zum gebundenen VWF:PP frei. Die Reaktion wird nach einer bestimmten Zeit gestoppt und die Absorption gemessen. Diese zeigt die Konzentration von VWF:PP an.
Der Assay wird durch parallele Messung des mitgelieferten Kalibrators und seiner Verdünnungen anhand einer Kalibrierungskurve kalibriert. Eine Qualitätskontrolle ist durch gleichzeitige Analyse des Kontrollplasmas möglich, das im Kit enthalten ist.
Produktnummer: 13.02.095.0096 (Abarbeitung mittels Pipettierroboter), 13.02.095.1096 (manuelle Abarbeitung)
Produktbezeichnung: INTER-ARRAY VFW:PP ELISA Kit – Enzymimmunoassay (ELISA) zur quantitativen Bestimmung des von-Willebrand-Faktor-Propeptids (VWF:PP) in humanem Blutplasma. Nur für Forschungszwecke.
Produktumfang: Das Ready-to-Use-Kit ist in zwei Versionen bei unseren Distributoren erhältlich: zur manuellen Abarbeitung im Labor oder für den Einsatz von Pipettierautomaten. Enthalten sind neben den einzeln verpackten mit Antikörpern beschichteten Mikrotiterplattenstreifen alle für die Abarbeitung benötigten Reagenzien sowie lyophilisiertes Kalibrator- und Kontrollplasma.
Literatur/ Datenblätter
Anfragen und Bestellungen
Bot. Tox. A Abicap SL 24 Kit / Bot. Tox. B Abicap SL 24 Kit
Immunoassay zum Nachweis von Botulinumtoxin A bzw. Botulinumtoxin B
Die verwendeten Abicap-Säulen enthalten drei 3-dimensionale Filter: Zwei Abstandsfilter (1,6 x 5 mm), die mit BSA beschichtet sind, und dazwischen einen Messfilter (2,5 x 5 mm), der mit gegen Botulinumtoxin A1/2 bzw. Botulinumtoxin B gerichteten Fängerantikörpern beschichtet ist.
Im ersten Schritt wird die vorinkubierte Probe auf die Abicap-Säule aufgetragen und von dem spezifischen Antikörper auf der Filteroberfläche eingefangen. Die Sandwich-Komplexe werden durch Zugabe von Streptavidin-Poly-Meerrettich-Peroxydase und Tetramethyl-Benzidin Substratlösung nachgewiesen. Die enzymatische Reaktion führt zu einem blauen Präzipitat auf der Filteroberfläche mit einer optischen Dichte, die proportional zur Toxinkonzentration ist.
Messbereich in Probenverdünnungspuffer: 5–100 U/ml bzw. 5–500 U/ml.
Produktnummer: 13.02.071.0240 (Bot. Tox. A Abicap SL 24 Kit) und 13.02.072.0240 (Bot. Tox. B Abicap SL 24 Kit)
Produktbezeichnung: Bot. Tox. A Abicap SL 24 Kit und Bot. Tox. B Abicap SL 24 Kit – Test-Kits für die Bestimmung von Botulinustoxin A bzw. Botulinustoxin B. Nur für Forschungszwecke.
Produktumfang: Enthalten sind neben den einzeln verpackten mit Antikörpern beschichteten Mikrofiltern beladenen Abicap-Säulen alle für die Abarbeitung benötigten Reagenzien.
Anfragen und Bestellungen
MMP9 Schnelltest
Lateral Flow Assay zum Nachweis von MMP-9 (Matrix-Metalloprotease 9) in Körperflüssigkeiten von Pferden
Verwendung
Der MMP-9 Kassettentest ist ein visueller Schnelltest zum qualitativen Nachweis von MMP-9 in Körperflüssigkeit von Pferden. Dieses Kit soll als Hilfe bei der Einschätzung der Proteasenaktivität dienen und ist nur für den in-vitro-diagnostischen Gebrauch durch professionelle Anwender gedacht.
Hintergrundinformationen
Matrixmetalloproteinasen (MMP) spielen bei degenerativen Prozessen eine Schlüsselrolle und sind damit ein prädestinierter Biomarker bei entzündlichen Erkrankungen des Pferdes (Clutterbuck et al. 2010). MMP-9 ist bei Gelenkerkrankungen ursächlich am Knorpelabbau beteiligt (Clegg und Carter 1999; Clegg et al. 1997) und wird deshalb bei Lahmheiten als Marker herangezogen. Auch bei Pferden mit Kolik-Symptomen und einem positiven Sepsos-Score sind die MMP-9 Konzentrationen in Plasma und Peritonealflüssigkeit erhöht (Barton et al. 2021).
Bei der operativen Behandlung der rezidivierenden Uveitis (ERU) mittels Vitrektomie kann mit Hilfe der MMP-9-Schnellanalyse ein intraoperatives Monitoring zur Einschätzung des OP-Fortschrittes erfolgen.
Mit dem für Pferde spezifischen MMP-9-Kassettentest können zeit-und arbeitsaufwändige Labormethoden wie Zymographie und ELISA umgangen werden und ein Ergebnis liegt nach wenigen Minuten vor. Zur exakten Quantifizierung des MMP-9-Gehaltes sollte allerdings der pferdespezifische MMP-9-ELISA durchgeführt werden.
Testprinzip
Der MMP-9-Test ist ein Sandwich-Immunoassay zum Nachweis von MMP-9 in Körperflüssigkeit von Pferden mittels visueller Interpretation der Farbentwicklung in der Testkassette. Die Membran wurde in der Testlinienregion (T) mit einem Antikörper gegen equines MMP-9 beschichtet. Während des Tests reagiert die verdünnte Probe mit einem gefärbten Konjugat (anti-equine-MMP-9-Antikörper-Goldkonjugat), das auf das Pad im Inneren der Testkassette gegeben wurde.
Das Gemisch bewegt sich chromatographisch mittels Kapillarwirkung über die Membran. Ist in der Probe MMP-9 vorhanden, bildet sich in der Testlinienregion (T) der Membran eine farbige Linie mit einem spezifischen Antikörper-Antigen-Konjugatkomplex. Dieser Komplex besteht aus einem gefärbten anti-MMP-9-Antikörper, MMP-9 aus der Probe und dem auf der Membran in der Testlinienregion (T) fixierten Antikörper.
Andererseits erscheint in der Kontrollregion (C) immer eine farbige Linie. Hierzu wird eine andere Antigen-Antikörperreaktion (mit Antimaus-Antikörpern) genutzt. Diese Kontrolllinie dient als Verfahrensindikator für die ordnungsgemäße Funktion des Tests. Sie zeigt an, dass das Testverfahren korrekt abgelaufen und die Probe ordnungsgemäß über die Membran geflossen ist.
Eine ausgeprägte Farbentwicklung in der Testlinienregion (T) zeigt ein positives Ergebnis an (MMP-9 in der Probe enthalten). Das Fehlen einer Farblinie in der Testlinienregion (T) weist auf ein negatives Ergebnis hin (kein MMP-9 in der Probe enthalten).
MMP9 ELISA
ELISA zum Nachweis von MMP9 (equine Matrix-Metalloprotease 9)
in Körperflüssigkeiten von Pferden
Produktbezeichnung: eqMMP-9 FAST ELISA Kit
Der MMP-9-ELISA ist ein immunologisch-enzymatisches Nachweisverfahren zum Nachweis von equiner Matrixmetalloproteinase 9 (eqMMP-9, Gelatinase B, 92 kDa Gelatinase, 92 kDa Type IV Collagenase, MMP-9) in Körperflüssigkeiten von Pferden.
eqMMP läßt sich in verschiedenen Körperflüssigkeiten von Pferden nachweisen u.a. in Synovialflüssigkeit, Glaskörperflüssigkeit und bronchoalveolärer Lavage Flüssigkeit (BALF).
Die im Kit eingesetzten monoklonalen Antikörper wurden gegen natives equines MMP-9 erzeugt.
Der ELISA ist zur Durchführung durch Fachpersonal im veterinärmedizinisch-diagnostischen Bereich geeignet.
Anfragen und Bestellungen
Über MMP-9
MMP-9, auch 92 kDa Typ IV Kollagenase, 92 kDa Gelatinase oder Gelatinase B genannt, ist bei vielen physiologischen Prozessen involviert und andererseits beim pathophysiologischen Abbau der extrazellulären Matrix beispielsweise im Gelenkknorpel bei Gelenkerkrankungen, im Glaskörper des Auges bei der equinen rezidivierenden Uveitis (ERU), in Peritonealflüssigkeit bei der Endotoxämie der equinen Kolik, in bronchoalveolärer Lavage-Flüssigkeit (BALF) bei Recurrent Airway Obstruction (RAO, COPD), in Wundexsudat bei Wundheilungsstörungen, bei Tumoren und anderen Krankheiten ursächlich beteiligt, weil überschießend aktiviert. Es ist damit ein prädestinierter Biomarker bei entzündlichen Erkrankungen des Pferdes.
Literatur
Clegg, P.D. and Carter, S.D. (1999) Matrix metalloproteinase-2 and -9 are activated in joint diseases. Equine Vet J 31, 324-330.
Clegg, P.D., Coughlan, A.R., Riggs, C.M. and Carter, S.D. (1997) Matrix metalloproteinases 2 and 9 in equine synovial fluids. Equine Vet J 29, 343-348.
Barnewitz, D., Karakine E., Richter I.-G., Lerchbacher J. (2015) Bedeutung der MMP-9 bei der Lahmheitsdiagnostik. Der praktische Tierarzt 96. Jahrgang, S. 1124 ff
Clutterbuck, A.L., Harris, P., Allaway, D. and Mobasheri, A. (2010) Matrix metalloproteinases in inflammatory pathologies of the horse. Vet J 183, 27-38.
Barton, A.K., et al. (2021). MMP-9 Concentration in Peritoneal Fluid Is a Valuable Biomarker Associated with Endotoxemia in Equine Colic. Mediators of Inflammation Vol. 2021.
fTLI ELISA
ELISA zum quantitativen Nachweis von felinem Trypsinogen in Serum
Als wichtigster Laborparameter für eine Pankreasinsuffizienz bei Katzen wird die feline Trypsin-like Immunoreactivity (fTLI) angesehen werden. Hierbei werden sowohl Trypsin als auch dessen Vorstufe, das Trypsinogen, im Serum bestimmt.

Produktbezeichnung: fTLI-ELISA
Produktumfang: fTLI-Kit je 10x
-
- 96 well-Mikrotiterplatte mit anti-fTLI beschichtetem Fängerantikörper
(einzeln entnehmbare Kavitäten oder Streifen)
-
- Verdünnungspuffer
- Waschpuffer
- Substratlösung
- Stopplösung
- Antikörperkonjugat (ready to use)
- Trypsinogen-Standard S1 (ready to use)
- Kontrollserum (fTLI 10 – 14 μg/L)
Preis: Auf Anfrage
Produktbeschreibung
Die Bestimmung der felinen trypsin-like immunoreactivity (fTLI) – Konzentration im Blutserum ist ein spezifischer Parameter für die exokrine Pankreasfunktion in der Labordiagnostik.
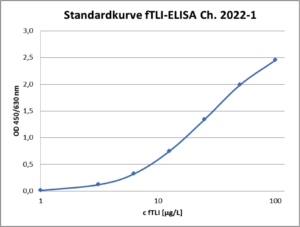
Der fTLI-Screening Test ist ein hoch spezifischer ELISA im Mikrotiterplattenformat zum quantitativen Nachweis von felinem Trypsinogen aus Serumproben. Die Bestimmung erfolgt direkt aus Serumproben von Katzen, ohne vorherige Isolation in einem Messbereich von 3 bis 100 µg/L. Das Testresultat ist bereits innerhalb von 90 min nach Probenauftrag ablesbar. Das spezielle ELISA-Setup ermöglicht eine einfache, wellgenaue und schnelle Probenanalyse mit geringem Handlingaufwand.
Anfragen und Bestellungen
Schnelltest für Nachweis von LukF-P83 in S.aureus
Bakterielle Infektionen des Euters
Mastitis ist eine entzündliche Erkrankung des Euters, die u.a. durch den Infektionserreger Staphylococcus aureus hervorgerufen wird. Eine frühzeitige Erkennung und Behandlung der Infektion ist entscheidend, um die Ausbreitung in der Milchviehherde zu verhindern.
Infektions-Nachweis über Schnelltest
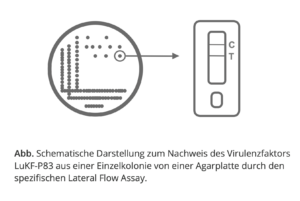
Die in Europa für die Mastitis relevanten Stämme von S. aureus können über das Genprodukt lukF-P83 (codiert für das Exotoxin Leukocidin) identifiziert werden. Wir haben daher einen einfach durchzuführenden Lateral Flow Assay entwickelt. Dieser Test ist spezifisch für das bakterielle Exotoxin (LukF-P83) von S. aureus.
Jetzt Aktionsangebot sichern
Wir unterstützen Ihre Arbeit mit der Produktion einer Serie von 500 Stück LukF- P83 Lateral Flow Assay (20 x 25 Antigen- Schnelltest) zum einmaligen Aktionspreis von 3.180,00 EUR anstatt 4.890,00 EUR zzgl. MwSt. und Versand.
Dieses Angebot ist gültig bis zum 30.09.2024.
Kontakt
Literatur
Schlotter K., Ehricht R., Hotzel H.; Monecke S., Pfeffer M., Donat K. 2012. Leukocidin genes lukF-P83 and lukM are associated with Staphylococcus aureus clonal complexes 151, 479 and 133 isolated from bovine udder infections in Thuringia, Germany. Veterinary research 43. https://doi.org/10.1186/1297-9716-43-42
Antikörper und Antigene
Übersicht Antikörper
Am fzmb entwickeln wir mittels Hybridomtechnik spezifische monoklonale Antikörper im Wirtsorganismus Maus. Neben der Antikörperherstellung können wir auch das äquivalente Antigen liefern (rekombinante und native Proteine, Peptide, Mikroorganismen und deren Strukturen).
Für eine schnelle Downstream-Entwicklung bieten wir die Charakterisierung der Antikörper und Matched Pair Analysen an. Die Antikörper können somit in qualitativ hochwertigen und effektiven Testsystemen Anwendung finden.
Neben den monoklonalen Antikörpern (Maus, Reinigung über Affinitätschromatografie) bieten wir auch die entsprechenden Hybridomzelllinien an. Unsere Produktion ist konform gemäß ISO 9001. Eine Produktion von Antikörpern unter ISO 13485 ist auf Anfrage möglich.
Monoklonale Polyhisitidin-Antikörper (6xHis-tag)
Polyhistidin-Tags werden z.B. zur Reinigung rekombinanter Proteine per Affinitätschromatographie eingesetzt. Die Anti-Polyhistidin-Tag-Antikörper eigenen sich z.B. für den Nachweis des His-Tag an diesen rekombinanten Proteinen.
Wir bieten verschiedene Zelllinien und Antikörper für Anti-Polyhistidin-Tag in unserem Geschäftsbereich mylab-Systemlösungen/Labor- und POCT-Diagnostik.
Monoklonale Legionellen-Antikörper
Legionellen sind gramnegative, aerobe Bakterien. Laut RKI sind über 60 Arten mit fast 80 verschiedenen Serogruppen bekannt.
Wir bieten verschiedene Zelllinien und Antikörper gegen verschiedene Servovare in unserem Geschäftsbereich mylab-Systemlösungen/Labor- und POCT-Diagnostik.
Monoklonale AK gegen Methicillin-resistente S. aureus
Methicillin-resistente S. aureus Stämme (MRSA) zeichnen sich dadurch aus, dass sie nicht nur gegen alle bisher marktverfügbaren β-Lactam-Antibiotika sondern auch gegen die Penicillase-stabilen Antibiotika Methicillin und Oxacillin resistent sind. Die Ursache dieser Resistenz liegt im mecA-Gen, welches ein modifiziertes Penicillin-Bindeprotein (PBP2a) codiert.
Panton-Valentine-Leukozidin (PVL) ist ein starker Virulenzfaktor von Staphylococcus aureus. Dieses Exotoxin führt zur Lysis von Leukozyten, in dem es Poren in der Zytoplasmamembran bildet. PVL-produzierende S. aureus-Erreger sind stark pathogen und verursachen schwere Infektionen der Haut und Weichteilgewebe bis hin zu letal verlaufenden Pneumonien.
Wir bieten die monoklonale Antikörper (inkl. matched pairs) und AK-produzierende Hybridomzelllinien gegen penicillin-binding protein 2a (PBP2a) und gegen Panton-Valentine-Leukozidin (PVL) in unserem Geschäftsbereich mylab-Systemlösungen/Labor- und POCT-Diagnostik an.
Monoklonale Antikörper gegen Paratuberkulose
Die Paratuberkulose, auch „Johne’sche Krankheit“ genannt, ist eine durch Mycobacterium avium ssp. paratuberculosis (MAP) hervorgerufene chronische entzündliche Darmerkrankung, die vorwiegend bei Wiederkäuern auftritt. Für einen immunologischen Nachweis der Paratuberkulose haben wir ein Set von Antikörpern entwickelt.
Wir bieten verschiedene monoklonale Antikörper und AK-produzierende Hybridomzelllinien gegen Mycobacterium avium ssp. paratuberculosis (MAP) in unserem Geschäftsbereich mylab-Systemlösungen/Labor- und POCT-Diagnostik an.
Monoklonale Antikörper gegen Mycotoxine
Mycotoxine, auch als „Schimmelpilzgifte“ bezeichnet, sind von Pilzen gebildete Stoffwechselprodukte die in Agrarprodukten und Lebensmitteln enthalten sein können. Bei Wirbeltieren können Mycotoxine schon in geringsten Mengen verschiedene Giftwirkungen entfalten. Eine durch Mycotoxine verursachte Erkrankung wird als Mycotoxikose bezeichnet. Die am häufigsten vorkommenden Mycotoxine sind die von der Gattung Fusarium gebildeten Mycotoxine Deoxynivalenol (DON) und Zearalenon (ZEA).
Über unseren Geschäftsbereich mylab-Systemlösungen/Labor- und POCT-Diagnostik bieten wir verschiedene monoklonale Antikörper und AK-produzierende Hybridomzelllinien gegen die von der Gattung Fusarium gebildeten Mycotoxine Deoxynivalenol (DON) und Zearalenon (ZEA) an.
Übersicht Antikörper-produzierender Zelllinien
Wir bieten eine Auswahl an Antikörper-produzierenden Hybridoma-Zelllinien (Maus). Wir freuen uns auf Ihr Interesse an der kommerziellen Nutzung. Für den Preis einer gewünschten Zelllinie nehmen Sie bitte Kontakt mit uns auf.
- Alpha1-Proteinase Inhibitor (Hund) gegen cannie alpha1PI
- Archaea ssp. (u.a. Methanosarcinae) gegen M. mazei Gs14, M.mazei DSM2053, M. flavesc.
- BBI gegen Bowman-Birk Inhbitor
- Clostridium botulinum Neurotoxin C gegen BoNT-C
- Coxiella Burnetii gegen Coxiella burnetii Phase I oder II
- DON gegen Deoxynivalenol
- Fluoreszenz-Farbstoffe und -Quencher gegen FITC, Dyeomics 405, Dyomics 495, Dyeomics Quencher Q1, Dyeomics Quencher Q3
- Faktor X gegen human factor X
- Faktor Xa gegen human faxctor Xa
- Faulbrut, amerikanische (AFB)
- felines Trypsinogen g
- Heparin Binding Protein gegen human Heparin
- HIS-Tag gegen poly6-HIS-Tag
- Legionella pneumophila gegen verschiedene Serogruppen von SG1 bis SG14
- Lunasin
- MAP gegen Mycobacterium avium paratuberculosis (inactivierte Zellen)
- eMMP9 gegen equine matrix metallo proteinase 9)
- NDV gegen Newcastle Disease Virus
- fNTproBNP (felines Natriuretic Brain Peptide)
- cNTproBNP (canines Natriuretic Brain Peptide)
- PMSG gegen equine pregnant mare serum gonadotropin
- S. aureus LukF-P83 gegen Panton valentin leukozidin LukF-P83
- S. aureus PVL gegen Panton valentin leukozidin LukF-PV
- Salmonella ssp. gegen Salmonella enterititis
Kontakt
PBP2a Antikörper zum Nachweis von MRSA
Meticillin-resistente S. aureus (MRSA)
Bei jedem vierten Menschen findet man das Gram-positive Bakterium Staphylococcus aureus auf Haut und Schleimhäuten. S. aureus ist in der Regel harmlos, kann aber vor allem bei geschwächten Menschen schwerwiegende Krankheiten wie Lungenentzündungen, Knochen- oder Herzklappeninfektionen verursachen.
Infektionen mit diesem Gram-positiven Bakterium werden mit Antibiotika aus der Gruppe der sogenannten Beta-Lactame behandelt. Die β-Lactam-Antibiotika, zu denen die Penicilline, Chephalosporine und Carpabeneme (externer Link Übersicht Antibiotika) gehören, verhindern den Neuaufbau der Zellwand von Gram-positiven Bakterien, sodass diese nicht mehr lebensfähig sind .
Ein immer größer werdendes Problem ist die Zunahme von S. aureus Stämmen, die resistent gegen β-Lactam-Antibiotika sind. Diese Stämme werden als Meticillin-resistente S. aureus (MRSA) bezeichnet.
Methicillin-resistente S. aureus (MRSA) zeichnen sich dadurch aus, dass sie nicht nur gegen alle bisher marktverfügbaren β-Lactam-Antibiotika sondern auch gegen die Penicillase-stabilen Antibiotika Methicillin und Oxacillin resistent sind.
Modifiziertes Penicillin-Bindeprotein (PBP2a) führt zu Resistenz
Die Ursache dieser Resistenz liegt am mecA-Gen, welches ein modifiziertes Penicillin-Bindeprotein (PBP2a, Penicilline Binding Protein-2a) kodiert. Diese Transpeptidase ist an der Verknüpfung der bakteriellen Zellwandbausteine beteiligt. β-Lactam-Antibiotika können aber an dieses modifizierte Penicillin-Bindeprotein nicht mehr binden und die Zellwandbiosynthese kann ungehindert ablaufen.
Neue Antikörper gegen PBP2a
Für einen selektiven Nachweis von Meticillin-resistenten S. aureus (MRSA) Stämmen hat das fzmb in Kooperation mit anderen Forschungseinrichtungen und Unternehmen sehr potente PBP2a Antikörper entwickelt.
Die PBP2a Antikörper aus unseren Hybridomzelllinen können z.B. in immunologischen Test wie Lateral Flow Assays (LFA) oder ELISA verwendet werden. Entsprechende matched pairs stehen zur Verfügung. Die Produktion der Antikörper erfolgt gemäß ISO 9001. Produktion gemäß ISO 13485 auf Anfrage.
Produktnummer: PBP-003a; PBP-004: PBP-006; PBP-007; PBP-012
Produktbezeichnung: Anti-PBP2a [MRSA] Antikörper, Maus monoklonal, affinitätsgereinigt
Kontakt
Rekombinantes equines MMP-9
Produkt-Nr. :
Produktbezeichnung: eqMMP-9 (rekombinant)
Produktbeschreibung: Rekombinantes equines MMP-9 Protein; Spezies: Pferd; geeignet für: SDS-PAGE, WB, ELISA
Produktumfang: lyophilisiertes rekombinantes Protein, 10µg
Preis: auf Anfrage
Datenblätter
Kontakt für Informationen/ Bestellung
Dr. Ina-Gabriele Richter
Tel. +49 (0)360 – 833 177
Natives equines MMP-9
Produktbezeichnung: eqMMP-9 (nativ)
Produktumfang: 1 Glas-Vial mit 0,14 µg lyophilisiertem Enzym (Chromatographie-gereinigt)
Preis: auf Anfrage
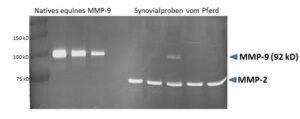
Produktbeschreibung
Natives equines MMP-9 Protein (aktiv); Spezies: Pferd; aktiv: ja, geeignet für: Funktionelle Studien (Zymographie, Gelatinase-Assay), SDS-PAGE, WB, ELISA; Chromatographie-gereinigt (Hibbs et al., 1985; Imai and Okada, 2008)
Literatur
Hibbs, M.S., K.A. Hasty, J.M. Seyer, A.H. Kang, and C.L. Mainardi. 1985. Biochemical and immunological characterization of the secreted forms of human neutrophil gelatinase. J Biol Chem. 260:2493-2500.
Imai, K., and Y. Okada. 2008. Purification of matrix metalloproteinases by column chromatography. Nat Protoc. 3:1111-1124
Datenblätter
PDF Product Certificate (engl.)
Anfragen und Bestellung
Dr. Ina-Gabriele Richter
Tel. +49 (0)3603 – 833 177
Kits für die Genotypisierung
INTER-ARRAY Genotyping Kit CarbaResist
Das Unternehmen INTER-ARRAY ist Bestandteil des fzmb. Das INTER-ARRAY Genotyping Kit CarbaResist ermöglicht den DNS-basierten Nachweis der häufigsten Carbapenemase-Gene von multiresistenten gramnegativen Bakterien aus Bakterienkulturen. Darüber hinaus ist auch die Identifizierung einiger wichtiger gramnegativer Bakterien (z. B. Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli) möglich.
Die Sonden für den Nachweis der Zielgene sind auf dem ArrayWell immobilisiert. Nach der Isolierung von RNS-freier, unfragmentierter genomischer DNS aus reinem und monoklonalem Koloniematerial wird die DNS unter Verwendung eines linearen PCR-Amplifikationsprotokolls und nur des Antisense-Primers der verschiedenen Targets amplifiziert und intern mit Biotin markiert.
Die Ergebnisse sind einzelsträngige DNS-Reaktionsprodukte (ssDNS). Im nächsten Schritt wird diese Biotin-markierte ssDNS auf den ArrayWell übertragen und auf DNS-Oligonukleotid-Mikroarrays mit 230 Sonden für verschiedene Carbapenemase- und AmpC-Gene sowie andere relevante Antibiotikaresistenz-Gene hybridisiert.
Nach der Hybridisierung und dem anschließenden Waschen bindet HRP-konjugiertes Streptavidin an die hybridisierten, mit Biotin markierten ssDNS-Stämme und macht sie in einer nachfolgenden enzymatischen Reaktion sichtbar. Die gleiche Reaktion findet mit der Färbekontrolle statt.
Die Auswertung der Spots und ihrer Intensitäten erfolgt automatisch auf der Basis eines digitalen Bildes des Microarrays mit dem INTER-VISION Reader. Die gesamte Probe wird automatisch auf das Vorhandensein oder Fehlen spezifischer Sonden analysiert, mit einer Datenbank abgeglichen und gibt dann Informationen über vorhandene Resistenzen und mögliche Bakterienarten aus.
Produktnummer: 13.02.102.0960
Produktbezeichnung: INTER-ARRAY Genotyping Kit CarbaResist – Test-Kits zur DNS-basierten Identifizierung bedeutender multiresistenter gramnegativer Bakterien sowie zur Charakterisierung wichtiger Carbapenemasen und anderer Resistenzen. Nur für Forschungszwecke.
Produktumfang: Die Abarbeitung des Genotypisierungskits ist in fünf Teilschritte gegliedert: Cell Lysis, DNA Labelling and Amplification, Hybridisation, Detection und Staining. Das Kit enthält Reagenzien zur Durchführung von 96 Einzelbestimmungen. Als Referenzmaterial ist DNS des E. coli-Stammes Nord8 im Kit enthalten.
Anfragen und Bestellungen
INTER-ARRAY Genotyping Kit S. aureus
INTER-ARRAY ist Bestanteil des fzmb. Das INTER-ARRAY Genotyping Kit S. aureus ermöglicht den DNS-basierten Nachweis von Resistenzgenen und Pathogenitätsmarkern von Staphylococcus aureus und die Zuordnung von unbekannten S. aureus-Isolaten zu bekannten Stämmen. Die Sonden für den Nachweis der Zielgene sind auf dem ArrayWell immobilisiert.
Nach der Isolierung von RNA-freier, unfragmentierter genomischer DNS aus reinem und monoklonalem S. aureus-Koloniematerial wird die DNS unter Verwendung eines linearen PCR-Amplifikationsprotokolls und nur des Antisense-Primers der verschiedenen Targets amplifiziert und intern mit Biotin markiert. Die Ergebnisse sind einzelsträngige DNS-Reaktionsprodukte (ssDNS).
Im Gegensatz zur Standard-PCR, bei der eine exponentielle Amplifikation stattfindet, ist die lineare Amplifikation weniger empfindlich und erfordert daher erheblich mehr DNS-Ausgangsmaterial (0,5-2 μg). Aus diesem Grund ist die Methode auf Koloniematerial beschränkt und kann nicht an Proben, z. B. aus Abstrichen, durchgeführt werden.
Im nächsten Schritt wird diese Biotin-markierte ssDNS auf ein ArrayWell übertragen und auf DNS-Oligonukleotid-Mikroarrays mit 336 Sonden für verschiedene genetische Marker von S.-aureus-Stämmen hybridisiert. Diese genetischen Marker umfassen eine Vielzahl von Speziesmarkern, virulenzassoziierte Gene für Exotoxine, Antibiotikaresistenz, MSCRAMMs, verschiedene Enzyme und andere Arten von Markern.
Nach der Hybridisierung und dem anschließenden Waschen bindet HRP-konjugiertes Streptavidin an die hybridisierten, mit Biotin markierten ssDNS-Stämme und macht sie in einer nachfolgenden enzymatischen Reaktion sichtbar. Die gleiche Reaktion findet mit der Färbekontrolle statt. Die Auswertung der Spots und ihrer Intensitäten erfolgt automatisch auf der Basis eines digitalen Bildes des Microarrays mit dem INTER-VISION Reader.
Das Gesamtmuster wird automatisch auf das Vorhandensein oder Fehlen spezifischer Marker analysiert und mit einer Datenbank von Stamm-Profilen verglichen, die die Zuordnung zu klonalen Komplexen und Stämmen ermöglicht.
Produktnummer: 13.02.101.0960
Produktbezeichnung: INTER-ARRAY Genotyping Kit S. aureus – Test-Kits zur DNS-basierten Bestimmung bakterieller Kulturen von Staphylococcus aureus-Isolaten. Nur für Forschungszwecke.
Produktumfang: Die Abarbeitung des Genotypisierungskits ist in fünf Teilschritte gegliedert: Cell Lysis, DNA Labelling and Amplification, Hybridisation, Detection und Staining. Das Kit enthält Reagenzien zur Durchführung von 96 Einzelbestimmungen. Als Referenzmaterial ist DNS des S. aureus-Stammes N315 im Kit enthalten.
Anfragen und Bestellungen
Vor-Ort-Messung: Inhaltsstoffe von Lebensmitteln

mylab NIR-Analyzer MEAT

Echtzeitüberwachung für Zusammensetzung von Fleisch- und Wurstwaren
Der mylab NIR-Analyzer MEAT ist ein hochpräzises dabei robustes und einfach zu bedienendes Messinstrument. Über ein spezielles bildgebendes Verfahren (Spektrometrie) wird die Zusammensetzung von Fleisch- und Wurstwaren analysiert.
Die aufgenommenen NIR-Spektren und deren automatischer Bewertung ermöglichen damit eine schnelle und kostengünstige vor-Ort-Analyse z.B. im Produktionsprozess. Die berührungs- und zerstörungsfreie Messung erfolgt innerhalb weniger Sekunden und benötigt keine zusätzlichen Chemikalien.
Der mylab-NIR Analyzer MEAT wird mit einer umfangreichen Grundkalibration für Fleisch- und Wurstwaren ausgeliefert. Eine Anpassung auf weitere Produkte ist jederzeit möglich.
Stärken des mylab NIR-Analyzers MEAT
- 21 in der Fleischwirtschaft relevante Parameter in wenigen Sekunden messbar
- kleine Standfläche und geringes Gewicht, flexibel einsetzbar
- einfach zu bedienende 1-Klick-Software
- kein Chemikalienverbrauch
- kostengünstig
Das mylab Gerät kann zudem auf spezielle Produkte angepasst werden.
Produkt-Nr.: P006-001
Produktbezeichnung: mylab NIR- Analyzer MEAT
Produktumfang: 1 mylab NIR- Analyzer MEAT inkl. Software und Kalibrationsmodellen (L 34 cm x B 24 cm x H 32 cm; 5,5 kg), Netzteil (1x), Netzkabel (1x), Ersatzlampe (1x), Petrischale aus Spezialglas (5x), Ersatz-Staubfilter (2x); Bedienungsanleitung; Gesamtgewicht: 10 kg inkl. Verpackung
Parameter
Bestimmung von 21 Paramentern für Fleisch- und Wurstwaren
- BIG 7 (nach EU-VO 1169/2011)
- pH-Wert
- aW-Wert
- BEFFE
- BEFFE im FE
- Fremdwasser (über Federzahl) u. andere
Die Grundkalibrierung umfasst die Produktgruppen Frischfleisch, Roh-, Brüh und Kochwurst von Rind und Schwein.
PDF Kalibrationsdatenblatt Fleisch und Wurstwaren (deutsch)
PDF Technische Spezifikationen (english)
Ansprechpartner für weitere Informationen
Alexander Mücke
+49(0)3603 – 833 193
Weitere Informationen finden Sie zudem unter
mylab NIR-Analyzer CF (custom-fit)
Echtzeitbestimmung für Zusammensetzung von Lebensmitteln
Der mylab NIR-Analyzer CF ist ein hochpräzises Instrument für die Analytik von Inhaltsstoffen von Lebensmitteln. Mittels aufgenommener NIR-Spektren und deren automatischer Bewertung ermöglicht das System eine schnelle und kostengünstige vor-Ort-Analyse im gesamten Produktionsprozess. Die berührungs- und zerstörungsfreie Messung erfolgt innerhalb weniger Sekunden und benötigt keine zusätzlichen Chemikalien.
Für die Anwendung benötigt der mylab NIR-Analyzer CF eine spezifische Kalibration für das jeweilige Produkt (z.B. Molkereiprodukte, Fertiggerichte, Feinkostsalate, Saatgut, Getreide, Mehl, Futtermittel, Kleintierfutter). Basierend auf unserer Datenbank (mit Kalibrationen) und in Ergänzung durch Kalibrationen Ihrer Produkte entsteht so ein hochpräzises Messverfahren.
Stärken des mylab NIR Analyzers CF
- Daten zu relevanten Parametern in wenigen Sekunden messbar
- kleine Standfläche und geringes Gewicht, flexibel einsetzbar
- einfach zu bedienende 1-Klick-Software
- kein Chemikalienverbrauch
- kostengünstig

Ansprechpartner für weitere Informationen
Alexander Mücke
+49(0)3603 – 833 193
Weitere Informationen finden Sie zudem unter

