Wir bieten diverse molekularbiologische, mikrobiologische und biotechnologische Untersuchungen und Entwicklungsleistungen an. Dabei kann es sich um Studien oder um die Umsetzung eines Vorhabens handeln. Wir begleiten Sie von der Idee eines neuen Produktes oder eines neuen Verfahrens bis zur Markteinführung.
Unser akkreditiertes Prüflabor (Abteilung für Lebensmitteluntersuchung) am fzmb bietet zudem eine Vielzahl von Dienstleistungen im Bereich von mikrobiologischen und chemischen Analysen.
Unser Geschäftsbereich Inter-Array bietet Spotting-Dienstleistungen z.B. für Multiparameter-Assays an.
Im Geschäftsbereich mylab-Systemlösungen finden Sie Geräte und Leistungen vor allem in Bereich von Qualitätskontrollen z.B. in der Produktion von Lebensmitteln.
Die Tierklinik bei uns am Institut versorgt große und kleine Tiere in nahezu allen medizinischen Bereichen. Neben der Kleintierpraxis liegt der Fokus unserer Tierklinik besonders auf der medizinischen Betreuung von Pferden.
Diagnostische Systeme

Entwicklung und Herstellung von Microarrays
Microarrays bestehen aus einer großen Anzahl von mikroskopisch kleinen Spots, die sich durch Hochpräzisionsdispensierer auf einer festen Oberfläche exakt aufbringen lassen. So können beispielsweise mehr als 700 Spots in einer einzelnen Kavität einer 96-Well-Mikrotiterplatte appliziert werden.
Kundenspezifische Entwicklung
Im Geschäftsbereich INTER-ARRAY am fzmb begleiten wir Sie durch alle Entwicklungsphasen von Microarrays von der Machbarkeitsstudie bis hin zur Pilotproduktion. Nach erfolgreicher Entwicklung stehen wir Ihnen mit unseren ISO-zertifizierten Fertigungskapazitäten als Contract Manufacturing Partner zur Verfügung.
Qualitätskontrolle von Microarrays
Der Fokus liegt auf der hohen Qualität der Microarray-Produkte. Für die Produktion arbeiten die Dispensiersysteme in einer klimatisierten Umgebung mit Inline-QC-Software, so dass eine Qualitätskontrolle aller produzierten Arrays gewährleistet ist.
Informationen
Weitere Informationen finden Sie auf unserer Website www.inter-array.com.
Ansprechpartnerin
Katrin Frankenfeld
Abteilungsleiterin Biotechnologie
Tel. +49 3603 – 833 141
Entwicklung und Produktion von Multiparameter-Tests
Die Protein- und Antikörper-Microarray-Technologie bietet enormes Potenzial für eine Vielzahl von diagnostischen Anwendungen. Miniaturisierte, parallelisierte Immunoassays sowie DNA-basierte Microarrays sind ideal, um mit kleinen Proben- und Reagenzienvolumina ein Maximum an diagnostisch relevanten Informationen zu generieren. Ein Microarray spart so viel Zeit, wertvolle Proben und teures Rohmaterial.
Anwendung in der in der Human- und Veterinärmedizin
Der Einsatz von Microarrays in der Human- und Veterinärdiagnostik ist für alle Anwendungen interessant, bei denen mehrere Analyten aus einer einzigen Probe bestimmt werden können.
Typische Beispiele für Multiparameter-Analytik sind Allergie- und Nahrungsmittelunverträglichkeitstests, die Diagnose von Autoimmun-, Stoffwechsel- und Infektionskrankheiten sowie die Krebsdiagnostik. Die Technologie bietet hervorragende Perspektiven für neue Wege der individualisierten Diagnostik und der personalisierten Medizin.
Multiparameter-Analytik in verschiedenen Formaten
Im Geschäftsbereich INTER-ARRAY am fzmb führen wir Neuentwicklungen von verschiedensten Multiparameter-Tests durch. Es können sowohl Standard-Detektionsformate wie ELISA, Lateral-Flow-Streifen und Mikrofluidik-Tests als auch kundenspezifische Plattformen verwendet werden.
Unser Team bietet eine flexible Unterstützung bei Machbarkeits-, Validierungs- sowie Produktionsprojekten für verschiedene Tests auf Basis von Microarrays an. Neben der kompletten Neuentwicklung ist auch die Übertragung bestehender Tests auf die Microarray-Plattform möglich.
Informationen
Weitere Informationen finden Sie auf unserer Website www.inter-array.com.
Ansprechpartnerin
Katrin Frankenfeld
Abteilungsleiterin Biotechnologie
Tel. +49 3603 – 833 141
Hochpräzisionsdispensieren
Um sehr kleine Volumina von Fängermolekülen (von Pikoliter bis Mikroliter) in hoher Präzision auf eine beliebige Oberfläche aufzubringen zu können, bedarf es neben sehr guter Dispensiersysteme viel Erfahrung. Unser Geschäftsbereich INTER-ARRAY am fzmb ist mit einer Vielzahl von hochmodernen Microdispensern ausgestattet und verfügt über langjähriges fachliches Know-How.
Von Design bis Datenanalyse: Exklusive Printing-Angebote
Mit unseren etablierten Technologien für das Hochpräzisionsdispensieren und unserer jahrelangen Erfahrung von Design bis Datenanalyse schaffen wir ein exklusives Printing-Angebot im Bereich Life Science. Diesen Rundum-Service bieten wir zu einem attraktiven Preis-/Leistungsverhältnis an. Dabei stehen die hohe Qualität und kurze Produktionszeiten im Vordergrund.
Spotting verschiedenster Substanzen
Zu den Substanzen, die gespottet werden können, gehören Antikörper, andere Proteine und Peptide, Oligonukleotide, Kohlenhydrate, Zellen und Zelllysate, Partikel und chemische Verbindungen sowie spezielle, kundenseitig bereitgestellte Moleküle. Die zu beschichtenden Substrate sind Glas- und Polymerobjektträger, Mikrotiterplatten und Mikrokavitäten, Membranen und mikrofluidische Chips, Wafer, Biosensoren sowie individualisierte Oberflächen.
Informationen
Weitere Informationen finden Sie auf unserer Website www.inter-array.com.
Ansprechpartnerin
Katrin Frankenfeld
Abteilungsleiterin Biotechnologie
Tel. +49 3603 – 833 141
Entwicklung von Immunoassays
Der Lateral Flow Assay (LFA) ist ein immunologischer Streifentest. Er kombiniert das Prinzip der Dünnschichtchromatografie mit einer Antikörper-basierten Nachweis (colorimetrisch, enzymatisch oder Fluoreszenz). Ein LFA ist die Grundlage für den kostengünstigen, hochsensitiven und zuverlässigen Nachweis von verschiedensten Analyten.
Als Point-of-Care-Test (POCT) finden Lateral Flow Assays vielfache Anwendung z.B. in der Immundiagnostik oder bei der Untersuchung von Umwelt- und Lebensmittelproben.
Der ELISA (Enzyme-linked Immunosorbent Assay) dient zum qualitativen und/oder quantitativen Nachweis eines Analyten (Antigens) in einer Probe. Zudem können viele Proben parallel und automatisiert in Laborumgebung analysiert werden.
Wir entwickeln LFAs und ELISAs von der Machbarkeit bis hin zur Kleinserie bzw. Vorbereitung zur Produktion in Großserie. Mit Hilfe dieser Immunoassays können verschiedenste Analyten in komplexen Probenmatrices diagnostisch nachgewiesen werden. Voraussetzung für eine sichere selektive Bindung des Analyten in einer flüssigen Phase oder Gewebeprobe sind hoch spezifische und affine monoklonale und polyklonale Antikörper. Deren Herstellung und anwendungsbezogene Charakterisierung ist eine unserer Kernkompetenzen.
Zuverlässiger Nachweis von biologischen Strukturen in hoher Sensitivität
Imunoassays können den gesuchten Analyten bis in den Nanogramm-Bereich z.T. auch Pikogramm-Bereich nach gewiesen werden. Dabei sind qualitative und quantitative Nachweise aus verschiedensten biologischen Proben mit komplexer Zusammensetzung ohne Vorbehandlung möglich.
Am fzmb werden schnelle hochspezifische Testsysteme mit colorimetrischem, fluoreszenz- oder chemilumineszenzbasiertem Readout für beliebige Parameter entwickelt.
Leistungsübersicht
- Entwicklung von ELISAs zum qualitativen Nachweis von Mikro- und Makromolekülen (Formate: indirekter ELISA, Sandwich-ELISA)
- Entwicklung von ELISAs zum qualitativen Nachweis der Analyten (Format: Sandwich-ELISA)
- Entwicklung von Lateral Flow Assays (LFA) zum qualitativen/ quantitativen Nachweis von Biomarkern
- Optimierung der Assay-Komponenten und Arbeitsschritte zugunsten der Sensitivität und Testschnelligkeit
- Validierung des entwickelten ELISA/ LFA
Kontakt
Hochsensitive 4in1/ 6in1 Kombi-Schnelltests
Der Lateral Flow Assay (LFA) ist ein immunologischer Streifentest. Er kombiniert das Prinzip der Dünnschichtchromatografie mit einer Antikörper-basierten Nachweis.
Am fzmb entwickeln wir LFAs von der Machbarkeit bis hin zur Kleinserie bzw. Vorbereitung zur Produktion in Großserie.
Mehr Informationen aus einem Schnelltest
Ist es Covid-19, RSV oder Influenza (A oder B)? Wenn sich mehr als eine Frage stellt, dann sollte die Antwort auch hinreichend sein. Wir haben daher für Lateral Flow Assays eine neue Plattform entwickelt. Auf dieser neuen Plattform können bis zu 6 verschiedene Tests in einem Lauf integriert werden (6in1 Kombitests).
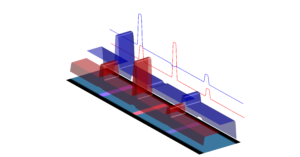
Einsatz von speziellen Nanopartikeln
Als Grundlage dienen spezielle fluoreszierende Nanopartikel, die wir mit dentsprechenden Antikörper konjugieren. Damit erreichen wir nicht nur das Multiplexen (mehrere Tests kombiniert). Die Empfindlichkeit (Nachweisgrenze des jweiligen Analyten) wird um das bis zu 10fache verbessert.
Das Auslesen der Kombi-Tests erfolgt digital mit einem entsprechenden Auslesegerät. Hierfür gibt es zwei Varianten: Für Laboranwendungen können handelsübliche Geräte (Lateral Flow Fluorescence Reader) verwendet werden. In Kooperation bieten wir für den Home-Use Einsatz auch serienreife Lösungen an.
PDF Hochsensitive Kombi-Schnelltests
Kontakt
Spezifische Antikörper
Herstellung monoklonaler Antikörper
Monoklonale Antikörper lassen sich für nahezu jedes beliebige Antigen bzw. Epitop generieren. Diese sind die Grundlage für die verschiedensten Immunologisch-basierten Nachweisverfahren, wie z.B. diagnostische ELISA-Tests. Anders als polyklonale Antikörper werden monoklonale Antikörper nur von einem Zellklon produziert (monoklonal) und binden damit hochspezifisch an das Epitop der gewünschten Zielstruktur.
Anwendungsbezogene Charakterisierung von monoklonalen Antikörpern
Zur Entwicklung von monoklonalen Antikörpern nutzen wir den Wirtsorganismus Maus. Mit Hilfe der Hybridomtechnologie, also der Fusion von Milzzellen und Myelomzellen, werden die Antikörper generiert.
Für eine schnelle Downstream-Entwicklung bieten wir gleich eine Charakterisierung der Antikörper sowie eine matched-pair-Analyse an. Dabei werden solche Paarungen von Detektor- und Fängerantikörpern ermittelt, die sich am besten für Ihr gewünschtes Testsystem eignen.
Auch Herstellung von Antigenen
Neben der Herstellung der Antikörper produzieren wir auch Antigene. Die Antigene können dabei rekombinante und native Proteine, Peptide oder Mikroorganismen sein und z.B. zur Entwicklung spezifischer Antikörper genutzt werden.
Die wichtigsten Vorteile auf einen Blick
- keine Chargenvarianz
- hohe Spezifität und Selektivität
- kontinuierliche Sekretion durch Hybridomzellkultur
Leistungsübersicht
- Herstellung/Beschaffung des Antigens
- Immunisierung von Versuchstieren (Maus)
- Überprüfung der Immunantwort (Titration der Seren)
- Generierung von antikörperproduzierenden Klonen mittels Hybridomtechnik
- Screening der Klone und Spezifitätstestung
- Charakterisierung der Antikörper (z.B. Isotypisierung, Expressionsleistung, Affinität zum Antigen)
- Etablierung der selektierten Klone als Zelllinie inkl. Kryokonservierung in Flüssigstickstoff
- Antikörperproduktion und -isolation mittels Affinitätschromatographie aus Zellkulturüberstand
- Integration in Immunoassays verschiedener Formate (ELISA, LFA, IFAT)
Kontakt
Übersicht monoklonale Antikörper-produzierende Zelllinien am fzmb
Antikörper gerichtet gegen
- Alpha1-Proteinase Inhibitor (Hund) gegen cannie alpha1PI
- Archaea ssp. (u.a. Methanosarcinae) gegen M. mazei Gs14, M.mazei DSM2053, M. flavesc.
- BBI gegen Bowman-Birk Inhbitor
- Clostridium botulinum Neurotoxin C gegen BoNT-C
- Coxiella Burnetii gegen Coxiella burnetii Phase I oder II
- DON gegen Deoxynivalenol
- Fluoreszenz-Farbstoffe und -Quencher gegen FITC, Dyeomics 405, Dyomics 495, Dyeomics Quencher Q1, Dyeomics Quencher Q3
- Faktor X gegen human factor X
- Faktor Xa gegen human faxctor Xa
- Faulbrut, amerikanische (AFB)
- felines Trypsinogen g
- Heparin Binding Protein gegen human Heparin
- HIS-Tag gegen poly6-HIS-Tag
- Legionella pneumophila gegen verschiedene Serogruppen von SG1 bis SG14
- Lunasin
- MAP gegen Mycobacterium avium paratuberculosis (inactivierte Zellen)
- eMMP9 gegen equine matrix metallo proteinase 9)
- NDV gegen Newcastle Disease Virus
- fNTproBNP (felines Natriuretic Brain Peptide)
- cNTproBNP (canines Natriuretic Brain Peptide)
- PMSG gegen equine pregnant mare serum gonadotropin
- S. aureus LukF-P83 gegen Panton valentin leukozidin LukF-P83
- S. aureus PVL gegen Panton valentin leukozidin LukF-PV
- Salmonella ssp. gegen Salmonella enterititis
Kontakt
Herstellung rekombinater Antikörper (Pferd)
In der Humanmedizin werden sogenannte chimäre (etwa 75 % humane) und humanisierte Antikörper seit mehr als 20 Jahren eingesetzt. Mittlerweile gibt eine Vielzahl zugelassener therapeutischer Antikörper für die humane Anwendung. Als der Tiermedizin sehr verbundenes Unternehmen haben wir uns die Entwicklung neuartiger immunologischer Therapien für Haustiere zur Aufgabe gemacht.
Spezifische Antikörper für die Therapie
Wir entwickeln rekombinante pferde-spezifische Antikörper für einen späteren therapeutischen Einsatz am Pferd. Aktueller Fokus dabei ist die Entwicklung eines Antikörpers gegen Matrixmetalloproteinase 9 (MMP-9). Dieser Antikörper soll als spezifisches Therapeutikum dienen beispielsweise zur gezielten Behandlung von Arthritis, Wundheilungsstörungen und equinem Sarkoid. Aber auch bei weiteren Krankheiten bei denen eine Überexpression der Matrixmetalloproteinase 9 (MMP-9) ursächlich beteiligt ist, soll eine neue Therapiemöglichkeit geschaffen werden. So können pathologische Prozesse, die aufgrund der gewebeabbauenden Eigenschaften von MMP-9 entstehen, gezielt am Ort der Entstehung gestoppt werden.
rekombinante Pferde-Immunglobuline
Für die Herstellung der equinen rekombinanten Antikörper wurden molekulargenetische Methoden entwickelt, um diese in Zellkultur zu produzieren. Diese Techniken können darüber hinaus genutzt werden, um weitere Pferde-Immunglobuline beispielsweise als passive Immuntherapeutika gegen Infektionskrankheiten des Pferdes herzustellen. Aufgrund der Wahl der Subtypspezifität und der regulatorischen Fc-Region kann über die gewünschte Antigenspezifität hinaus das Potential als Modulator genutzt werden, das körpereigene Immunsystem, z.B. gegen eine bestehende Krebserkrankung, zu stärken.
Gehen Sie mit uns Gespräch über Ihr Anliegen und Fragestellung. Unser Bestreben ist es, mit Ihnen gemeinsam die Grundlagen für eine innovative und spezifische Immuntherapie für das Pferd zu schaffen.
Wenn wir Ihr Interesse geweckt haben, kontaktieren Sie uns gerne.
Kontakt
Dr. Ina-Gabriele Richter
Tel. +49 3603 – 833 177
Herstellung von polyklonalen Antikörpern
Wir stellen artifizielle humane Immunseren mittels in-vitro-Immunisierung her.
Kontakt
Dr. Ina-Gabriele Richter
Tel. +49 3603 – 833 177
Passende Matched Pair Antikörper
Ob ein gewähltes matched-pair Antikörperpaar in einer geplanten Anwendung gut funktioniert, hängt von vielen Faktoren ab und läßt sich nicht vorraussagen.
Wir bieten daher nicht nur die Entwicklung spezifischer monoklonaler Antikörper (inklusive Findung passender Antikörperpaare (matched pair) für bspw. Immunoassay-Entwicklungen an.
Für eine bestmögliche Leistungsfähigkeit eines Matched Antibody Pair prüfen wir die Leistungsfähigkeit dieser Antikörper-Paare in der gewünschten Anwendung. Diese frühzeitige Testung der Antikörper in der Zielanwendung (ELISA, LFA mit Immunogold- bzw. Fluoreszenznanopartikeln, IFAT) ermöglicht eine gezielte Antikörper-Selektion bzw. -Entwicklung und erlaubt so die bestmögliche Performance.
Leistungsübersicht
- Entwicklung monoklonaler Antikörper gegen gewünschte Ziel-Strukturen
- Antikörper-Charakterisierung (Isotypisierung, Expression)
- Matched Pair Analyse im Zielformat (Sandwich-ELISA, Lateral Flow Assay LFA):
- Kopplung an Strukturen zum colorimetrischen oder fluorimetrischen Nachweis (Biotin, HRP, AP, Fluorenzenzfarbstoffe)
- Immobilisierung der Fänger-Kandidaten
- Detektoren-Analyse
- Testung möglicher Kombinationen
- Pufferoptimierung
Kontakt
Analytik von Lebensmitteln, Trinkwasser und Kosmetik

Labor für Lebensmitteluntersuchungen
Das Prüflabor in der Abteilung Lebensmitteluntersuchung am fzmb ist seit 1994 unabhängiger Dienstleister für Lebensmittelsicherheit und Verbraucherschutz. Das Labor ist durch die Deutsche Akkreditierungsstelle (DAkkS) nach DIN EN ISO 17025 akkreditiert.
Welche Produkte analysieren wir?
- Fleisch und Fleischerzeugnisse
- Milch und Milchprodukte
- Speiseeis
- Backwaren
- Getreide und Getreideerzeugnisse
- Feinkostsalate
- Fisch
- verzehrfertige Speisen
- Trinkwasser
- andere Produkte auf Anfrage
Welche Leistungen bieten wir an?
Lebensmittelmikrobiologie
- Prüfung gemäß gesetzlicher Vorgaben nach VO (EG) Nr. 2073/2005 bzw. gemäß Vorgaben der Deutschen Gesellschaft für Hygiene und Mikrobiologie (DGHM) für Produkte auf Handelsebene
- Oberflächenkeimgehalt auf Schlachtkörpern
- Pathogenmonitoring mittels PCR
- Salmonella-Antikörper in Fleischsaft und Serum
Betriebshygiene
- Kontrolle der Reinigung/ Desinfektion
- Kontrolle der Personalhygiene
- Luftkeimgehalt (incl. Probenahme)
- Pathogenmonitoring
Lebensmittelchemie
- Mykotoxine (Ochratoxin A)
- Hauptinhaltsstoffe
- Nährwerte
- Nitrit/ Nitrat
chemisch-physikalisch
- aw-Wert
- pH-Wert
- Schutzgasmessung
Trinkwasser
- Probennahme
- Mikrobiologie gemäß Trinkwasserverordnung
sonstige Dienstleistungen
- Probenabholung im modernem Kühlfahrzeug
- Prüfung der Deklaration auf Rechtskonformität
- Sensorische Prüfung
- Hygieneschulungen
- Betriebsbegehungen/ Hygieneaudits
- Gegenprobengutachten
- Beratung und Hilfestellung bei lebensmittelrechtlichen Fragestellungen sowie der Lösung
konkreter Probleme in folgenden Bereichen:
- Entwicklung, Produktion, Lagerung, Kennzeichnung und Inverkehrbringen von Lebensmitteln.
PDF Liste der Prüfverfahren Abteilung Lebensmitteluntersuchung
Kontakt
Steffi Leuschke
Staatlich geprüfte Lebensmittelchemikerin
Tel. +49 3603 – 833 173
Mikrobiologische und chemische Untersuchgung von Lebensmitteln
Als akkreditiertes Prüflabor führen wir mikrobiologische, chemische und chemisch-physikalische Untersuchung von Lebensmitteln durch, produktspezifisch u.a. auf:
- Krankheitserreger
- Verderberreger
- Einhaltung gesetzlicher Vorgaben (z.B. VO 2073/2005, Zusatzstoff-Zulassungsverordnung, Käseverordnung)
- Einhaltung von mikrobiologischen Richt- und Warnwerten der Deutschen Gesellschaft für Hygiene und Mikrobiologie (DGHM)
- aw-Wert und pH-Wert
- Bestimmung von Lebensmittelinhaltsstoffen
- Einhaltung von Vorgaben der Leitsätze des Deutschen Lebensmittelbuches
- Nährwertbestimmung „BIG 7“
- Bestimmung von Ochratoxin A in Getreide und Getreideprodukten mittels HPLC
- Nachweis von Antikörpern gegen Salmonella-Serovaren der Gruppen B, C, D und E in Fleischsaft und Bluterzeugnissen mittels ELISA, Eintrag der Ergebnisse in die Datenbank Qualiproof
- Prüfung von Kennzeichnungen auf Rechtskonformität
PDF Prüflabor für Lebensmittel
Kontakt
Steffi Leuschke
Staatlich geprüfte Lebensmittelchemikerin
Tel. +49 3603 – 833 173
Mikrobiologische Untersuchung von Kosmetik
Die mikrobiologische Produktsicherheit gehört zu den wichtigsten Faktoren der Sicherheitsbewertung von kosmetischen Mitteln. Unser Analyselabor prüft die mikrobiologische Qualität von kosmetischen Produkten sowie der eingesetzten Rohstoffe. Im Rahmen des betrieblichen Hygienemonitorings bieten wir für Hersteller von Kosmetika verschiedene Prüfungen von Prozesswasser bzw. Produktionswasser, von Raumluft und Oberflächen sowie von Packmaterialien an.
Das Spektrum unseres Labors umfasst folgende Analysemethoden:
- Konservierungsbelastungstest
(Beurteilung der Konservierung von kosmetischen Rezeptu-
ren)
- Prüfung auf mikrobielle Verunreinigung
- Nachweis spezifischer Mikroorganismen
- Überprüfung der Reinigung und Desinfektion von Oberflächen und Bedarfsgegenständen
- Überprüfung der Raumluftqualität
Kontakt
Steffi Leuschke
Staatlich geprüfte Lebensmittelchemikerin
Tel. +49 3603 – 833 173
Untersuchung von Luft, Gegenständen, Umgebungsproben
- Überprüfung der Reinigung und Desinfektion von Oberflächen und Bedarfsgegenständen
- Überprüfung der Raumluftqualität
- Überprüfung der Personalhygiene
Kontakt
Steffi Leuschke
Staatlich geprüfte Lebensmittelchemikerin
Tel. +49 3603 – 833 173
Untersuchung von Trinkwasser
Trinkwasser ist ein Lebensmittel und unterliegt daher strengen Regularien. Die Untersuchung von Trinkwasser in unserem Labor erfolgt gemäß der Verordnung über die Qualität von Wasser für den menschlichen Gebrauch (Trinkwasserverordnung – TrinkwV 2001).
Als akkreditiertes Prüflabor (zugelassene Untersuchungsstelle nach § 40 Abs. 1 der TrinkwV) überprüfen wir gerne, ob die Qualität Ihres Trinkwassers der Richtlinie 98/ 83 EG entspricht.
- Überprüfung der mikrobiologischen Trinkwasserqualität (Koloniezahl bei 22°C und 36°C, coliforme Keime, Escherichia coli, Enterokokken)
Zusätzlich bieten wir an:
- Bestimmung von Pseudomonas aeruginosa
- Bestimmung von Clostridium perfringens
- Prüfung von Trinkwasser-Installationen auf Legionella spp.
Hinweis: Wenn die Untersuchung Ihres Trinkwassers behördlichen Vorgaben genügen muss, bedarf es einer Probennahme durch unser akkreditiertes Personal.
Kontakt
Steffi Leuschke
Staatlich geprüfte Lebensmittelchemikerin
Tel. +49 3603 – 833 173
Biologische Wertstoffe
Inaktivierung von Bakterien und Viren
Die Verwendung von inaktivierten Mikroorganismen als Kontrollmaterial oder zur Immunisierung für die Antikörperproduktion kann die Gefahr von Infektion und Kontamination minimieren. Hierfür werden die entsprechenden Mikroorganismen durch eine spezielle UV-Behandlung inaktiviert.
UV-Inaktivierung von Mikroorganismen
UV-inaktivierte Bakterien und Viren sind besonders gut als mikrobiologisches Kontrollmaterial für wissenschaftliche oder medizinische Zwecke geeignet. Das energiereiche UV-Licht schädigt die DNA und bewirkt damit deren Inaktivierung. Die makromolekulare äußere Oberfläche bleibt jedoch erhalten. UV-inaktivierte Bakterien sind daher äußerst zweckdienlich zur Erzeugung von Antikörpern gegen Oberflächenantigene.
Werden inaktivierte Bakterien als Referenzmaterial zu vitalen Bakterien verwendet, so werden vergleichbare Ergebnisse erzielt. Auch zur Evaluierung molekularer Tests sind UV-inaktivierte Mikroorganismen als standardisierte, unabhängige Qualitätskontrollen ideal.
Inaktivierung nach Ihren Vorgaben
Wir bieten UV-inaktivierte Mikroorganismen als Ganzzellpräparate (z.B. inaktivierte Bakterien wie Legionellen oder Streptokokken oder auch andere Spezies gemäß BSL1 und BSL2). Sie erhalten die UV-inaktivierten MOs in Suspension mit einer eingestellten Zellzahl und bestimmen die gewünschten Puffer und Zusätze.
Nehmen Sie gerne mit uns Kontakt auf, damit wir Ihr individuelles Anliegen besprechen können.
Literatur
Mertens-Scholz, K., Moawad, A. A., Liebler-Tenorio, E. M., Helming, A., Andrack, J., Miethe, P., Neubauer, H., Pletz, M. W., Richter, I. G., (2024). Ultraviolet C inactivation of Coxiella burnetii for production of a structurally preserved whole cell vaccine antigen. BMC Microbiol 24(1): 118.
Informationen als PDF
Kontakt
Dr. Ina-Gabriele Richter

Tel. +49 3603 – 833 177
Inaktivierung von Baktieren und Viren
Die Verwendung von inaktivierten Mikroorganismen als Kontrollmaterial oder zur Immunisierung für die Antikörperproduktion kann die Gefahr von Infektion und Kontamination minimieren. Hierfür werden die entsprechenden Mikroorganismen durch thermische, chemische oder UV-Behandlung inaktiviert.
Kundenspezifische Inaktivierung
Wir bieten inaktivierte Mikroorganismen als Ganzzellpräparate (z.B. inaktivierte Bakterien wie Legionellen oder Streptokokken) als standardisierte, unabhängige Qualitätskontrollen zur Evaluierung molekularer Tests. Darüber hinaus können wir eine kundenspezifische Inaktivierung z.B. von Bakterien nach Ihren Vorgaben durchführen. Sie bestimmen die gewünschten Konzentrationen, Puffer und Zusätze.
Nehmen Sie gerne mit uns Kontakt auf, damit wir Ihr individuelles Anliegen besprechen können.
Thermische Inaktivierung von Bakterien und Viren
Anders als durch eine UV-Bestrahlung können mit unserem thermischen Verfahren auch größere Mengen an Mikroorganismen in kurzer Zeit inaktiviert werden. Die speziellen Bedingungen für die Inaktivierung sind dabei abhängig von der Art des Organismus.
Inaktivierte Bakterien sind bespielsweise besonders gut zur Erzeugung von Antikörpern gegen Oberflächenantigene geeignet. Werden inaktivierte Bakterien als Referenzmaterial zu vitalen Bakterien verwendet, so werden vergleichbare Ergebnisse erzielt.
Informationen als PDF
Kontakt
Dr. Ina-Gabriele Richter

Tel. +49 3603 – 833 177
BioCellulose (Made in Germany)
Ultradünn & ultraleicht
Natürliches Hautgefühl
Unsere BioCellulose ist ein reiner Naturstoff. Sie ist deutlich reiner als Pflanzenzellulose und besteht aus einem stabilen Geflecht ultradünner Fasern, die sich perfekt an jede Hautkontur anpassen. Die Masken sind besonders leicht und transparent und deshalb sogar für alle die interessant, die bislang keine Vliesmasken angewendet haben.
BioCellulose als Wirkstoffträger
In ihrem Geflecht aus Millionen von feinen Fasern speichert unsere BioCellulose kosmetische Wirkstofflösungen zur Behandlung und Pflege der Haut. Durch die optimale Anpassung an die Hautoberfläche werden die Wirkstoffmoleküle gezielt an die Haut abgegeben und sehr gute kosmetische Ergebnisse erzielt.
Anwendung
Einfache Anwendung im Kosmetikstudio oder zu Hause
Die BioCellulose-Masken sind unglaublich leicht und dünn. Dadurch liegen sie nahezu unsichtbar auf dem Gesicht auf. Die Anwendung der Masken ist sehr einfach. Das verwendete Trägermaterial erlaubt eine einfache Applikation der BioCellulose auf der Haut. Die zwei Maskenteile ermöglichen eine Anpassung an jede Gesichtsgröße. Durch die extrem gute Haftung der BioCellulose an der Gesichtsoberfläche hat der Kunde während der Behandlung eine hohe Bewegungsfreiheit.
Ideale Kombination mit apparativen Behandlungsmethoden
Die BioCellulose Masken stellen eine einzigartige Basis für die Kombination mit apparativen Behandlungsmethoden dar. Das Material der Masken erlaubt neben einer optimalen Wirkstofffreigabe eine perfekte Übertragung der physikalischen Effekte, um so Regenerationsvorgänge der Haut positiv zu beeinflussen und Stoffwechselvorgänge anzuregen.
Produktion
Entwicklung, Produktion und Verpackung
Wir agieren als Auftragsproduzent für die Herstellung von Kosmetikmasken nach Kundenwunsch. Unsere BioCellulose wird in Deutschland biotechnologisch aus Traubenzucker gewonnen und zu Masken verarbeitet. Wir imprägnieren die Masken mit den Wirkstoffen unserer Kunden oder stellen eine Produktformulierung bereit. Wir beraten gerne bei der Wirkstoffauswahl.
Forschung und Entwicklung
Wir setzen die Ideen um, die unsere Kunden an uns herantragen. Das Anfertigen von Mustern ist Bestandteil unseres Serviceangebotes. Durch eigene, perfekt ausgestattete Laboratorien sind unsere kompetenten Chemiker, Biologen und Laboranten in der Lage, umfangreiche Forschungs- und Entwicklungsdienstleistungen anzubieten.
Qualität
Wir produzieren seit 20 Jahren BioCellulose auf höchstem Niveau. Unser erfahrenes Team arbeitet zur Herstellung qualitativ hochwertiger Produkte nach anspruchsvollen Standards. Die GMP-konforme Produktion ist nach DIN ISO 9001 zertifiziert. Das Produkt ist dermatologisch getestet und wird komplett in Deutschland hergestellt. Wir garantieren eine schnelle Auftragsbearbeitung.
Kontakt
Dr. Ina-Gabriele Richter
Tel. +49 3603 – 833 177
Data Science & Optische Analytik

Hyperspektral-Imaging (HSI)
Qualitätskontrolle von Produktionsflüssen
Ein wichtiges Anwendungsfeld des Hyperspektral-Imagings ist die Qualitätskontrolle z.B. in der Lebensmittelproduktion. Die schnelle und kontinuierliche Datenerfassung und die Auswertung in Echtzeit schafft eine hervorragende Basis für Inline-Kontrollen von Produktionsflüssen. Beispiele hierzu finden Sie auf hier.
Hyperspektrales Imaging (HSI)
Jede Oberfläche und jedes Material besitzt eine eigene spektrale Signatur. Diese charakteristische Signatur kann mit einer Hyperspektralkamera aufgenommen werden. Algorithmen werten die Signaturen aus und ordnen sie qualitativen und quantitativen Eigenschaften der Messobjekte zu.
Funktionsweise HSI
Wie bei einem Scanner nehmen viele Hyperspektralkameras ihre Bilder zeilenweise auf. Dafür wird die zu untersuchende Probe unter der Kamera verschoben. In jedem erfassten Bildpunkt wird dabei ein charakteristisches Spektrum des Messobjektes innerhalb eines definierten Wellenlängenbereichs detektiert.
Datenauswertung in Echtzeit
Moderne Auswertungsverfahren erlauben es in Echtzeit, aus den hochkomplexen Messdaten sehr detaillierte Informationen über das Messobjekt zu generieren. So kann beispielsweise die quantitative chemische Zusammensetzung von Lebensmitteln bestimmt werden. Die Methode ermöglicht außerdem die Detektion von Fremdkörpern sowie die Erkennung von Qualitätsabweichungen oder Kontaminationen einzelner Objekte im Produktionsfluss. Die kontinuierliche Datenerfassung- und Auswertung ermöglicht eine vollständige Erfassung des gesamten Produktflusses. Die oft aufwändige und nicht repräsentative Entnahme von Stichproben entfällt.
HSI-Integration in Ihren Betrieb
Mit unseren HSI-Modulen können Objekte von wenigen Mikrometer bis zu 60 cm im Wellenlängenbereich von 400 – 2500 nm analysiert werden. Unser Labor führt zunächst Voruntersuchungen Ihrer Messobjekte und Materialproben durch. Auf Basis der Ergebnisse konfigurieren wir für Sie ein maßgeschneidertes In-Prozess-System unter Einbindung spezieller KI-basierter Auswertungsverfahren.
PDF Hyperspektral-Imaging
Kontakt
Florian Meuche
Abteilungsleiter Geräteentwicklung
Tel. +49 3603 – 833 194
NIR-Spektroskopie
Organische Proben absorbieren Licht im nahinfraroten (NIR) Wellenlängenbereich von 800-2500nm. In der Probe enthaltene Stoffe wie z.B. Proteine, Fette, Zucker und Wasserbestandteile erzeugen dabei ein charakteristisches NIR-Spektrum. Die Analytik kann sowohl qualitativ als auch quantitativ durchgeführt werden. Auch physikalische Parameter wie die Partikelgröße oder der pH-Wert beeinflussen die Form des NIR-Spektrums und lassen sich bestimmen.
Die NIR-Spektroskopie bietet damit schnelle, berührungslose und präzise Messergebnisse z.B. im Bereich der Lebens- und Futtermittelindustrie. Im Vergleich zu chemischer Analysen sind die NIR-Messungen sehr viel schneller (>60 sec), benötigen keine besondere Probenvorbereitung und können eine Vielzahl pro Parameter parallel analysieren.
Funktionsweise NIR-Spektroskopie
Durch die spezielle Anregung der Probe werden charakteristische Molekülschwingungen angeregt. Die Schwingungszustände innerhalb der Probe spiegeln sich im detektierten NIR-Spektrum wider. Eine Analyse der Form und Lage des gemessenen Spektrums ermöglicht eine Berechnung der chemischen Zusammensetzung/ physikalischen Parameter der Probe.
Integration der NIR-Spektroskopie in Ihren Betrieb
Zunächst werden Ihre Proben in unserem Spektroskopielabor vermessen. Parallel werden Ihre gewünschten Zielparameter in unserem akkreditierten Analyse-Labor bestimmt.
Dann wird das NIR-Spektrometersystem mylab-NIR Analyzer und Auswertungsmodel auf Ihre Messaufgabe optimiert. Die Integration in Ihren Produktionsablauf erfolgt individuell zugeschnitten auf Ihre Anforderungen.
Kontakt
Florian Meuche
Abteilungsleiter Geräteentwicklung
Tel. +49 3603 – 833 194
Ionenmobilitäts-Spektrometrie (IMS)
Schnelle Analytik von flüchtigen Stoffen
Die Ionenmobilitätsspektrometrie (IMS) analysiert flüchtige Verbindungen auf ihre chemische Zusammensetzung. Sie zeichnet sich durch niedrige Nachweisgrenzen (unterer ppb-Bereich) und kurze Messzeiten (ca. 20 sec) aus.
Funktionsweise IMS
Durch definiertes Erhitzen der Probe werden die chemischen Substanzen in die Gasphase gebracht. Die nun gasförmigen Substanzen werden zunächst in der IMS ionisiert. Angetrieben durch ein elektrisches Feld bewegen sich die Ionen durch eine gasgefüllte Röhre (Driftröhre).
In der Driftröhre treffen die Ionen auf Gasmoleküle (z.B. Luft). Je größer die Ionen einer Probe sind, desto häufiger kollidieren sie mit den Gasmolekülen und desto länger benötigen sie für die Passage durch die Driftröhre.
Nach der Passage durch die Driftröhre bestimmt ein Detektor die Driftzeit. Je länger die Driftzeit desto größer ist das Molekulargewicht eines Ions.
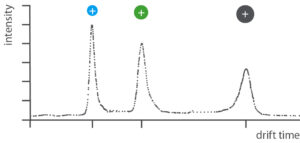
Untersuchung komplexer Gasproben
Zur Untersuchung komplexer gasförmiger Proben bietet sich die Probenvortrennung mittels Gaschromatografie (GC) an. Die am fzmb etablierte Gerätekonfiguration erlaubt die Analyse von leichten bis mittelflüchtigen Verbindungen bis zu einem Siedepunkt von 120 C°.
Die Bandbreite an analysierbaren Substanzen umfasst organische Verbindungen wie Kohlenwasserstoffe, Aldehyde, Ketone, Alkohole, Ester und Amine.
Datenauswertung
Die Auswertung der IMS Daten beinhaltet die Erkennung von Mustern in den gemessenen Spektren. Diese Mustererkennung hilft bei der Zuordnung von Ionen zu bestimmten Verbindungen und der Identifizierung unbekannter Substanzen. Durch die Erstellung von Klassifikationsmodellen wird die Präzision der Analytik verbessert.
Weitere Datenauswertungen betreffen die Konzentrationsbestimmung der analysierten Verbindungen. Dazu werden die Intensitäten der Ionenpeaks gemessen und mit Kalibrierstandards oder internen Standards verglichen. So gewonnene Daten werden für Regressionsmodelle genutzt.
weitere Informationen
Mehr zum Thema Ionenmobilitäts-Spektrometrie finden Sie hier.
Leistungsspektrum
- Fingerprint-Analytik
Vergleichende Analytik zweier sich unterscheidender Proben
(z.B. gesund vs. krank, behandelt vs. unbehandelt)
Unterschung zur Identifikation von differentiell exprimierten Substanzen
- Identifikation von unbekannten Substanzen (u.a. mittels GC-MS)
- Quantitative Analytik von bekannten (bzw. zurvor charakterisierten) Substanzen
IMS-Intergation in Ihren Betrieb
Anwendungsgebiete am fzmb:
- Mikrobiologie und Diagnostik von Infektionen
- Fortpflanzungsmedizin beim Nutztier
- Medikationsnachweis bei Sportpferden und bei Lebensmittel liefernden Tieren
- Nachweis von Inhaltsstoffen in tierischen Geweben
- Nachweis von Verunreinigungen und Zusätzen in Kunstoffen
PDF Ionenmobilitätsspektrometrie
Kontakt
Florian Meuche
Abteilungsleiter Geräteentwicklung
Tel. +49 (0)3603 – 833 194
Entwicklung von optischen Messgeräten: Machbarkeitsstudien und Validierungen
Optische Messgeräte
Die Zusammensetzung und Oberflächenbeschaffenheit von Materialen kann durch Wechselwirkungen zwischen Licht und Materie charakterisiert werden. Moderne optische Analysegeräte nutzen die physikalische Effekte wie Absorption, Reflexion, Transmission oder die Streuung von Licht zur Messung bestimmter Eigenschaften einer Probe.
Kluge Entwicklung spart Kosten
Zur Entwicklung effizient arbeitender und kostenoptimierter optischer Analysegeräte ist die genaue Kenntnis der optischen Eigenschaften der zu untersuchenden Proben unerlässlich. Auf Basis dieser Kenntnisse lassen sich optimal zugeschnittene technische Lösungen konzipieren. Damit können sowohl die Entwicklungszeit als auch die Kosten (u.a. für Hardware) reduziert werden.
State-of-the-Art Versuchslabor und Expertise
Mit unserem umfangreich ausgestattetem Spektroskopie-Labor, unserer Expertise auf dem Gebiet der optischen Messtechnik, moderne Simulationswerkzeuge und innovative KI-basierte Auswertungsmethoden unterstützen wir Sie bei der Entwicklung optimierter optischer Mess- und Analysegeräte.
Unsere Leistungen
- Messung von Absorption, Reflexion, Transmission und Streuung im Wellenlängenbereich von 200 – 4000 nm (UV – MIR) zur Identifikation problemrelevanter Wellenlängen
- Simulation der Lage und Leistung von Lichtquellen zur Auswahl geeigneter Bauelemente
- Simulationen zur Optimierung von Strahlengängen
- Simulation benötigter Detektorflächen für Photodioden
- Beratung zur Auslegung elektronischer Schaltungen zur Signalerfassung und Aufbereitung
Kontakt
Florian Meuche
Abteilungsleiter Geräteentwicklung
Tel. +49 3603 – 833 194
Übersicht Leistungen
- Messung von Absorption, Reflexion und Transmission im Wellenlängenbereich von 200 – 2.800 nm
- Streulichtmessungen
- zeitaufgelöste Fluoreszenzspektroskopie
- Nahinfrarotspektroskopie
- Hyperspektrale Messungen im Wellenlängenbereich von 400 – 2.500 nm
- Entwicklung chemometrischer Modelle für die NIR-Spektroskopie
- Entwicklung KI-basierter Auswertungsverfahren für hyperspektrale Messdaten
- strahlenoptische Simulationen
- CAD-Modellierung und 3D-Druck
Übersicht Geräteausstattung
- Stratasys OBJET 30 Prime Desktop 3D-Drucker
- Ocean Optics HR4000 CG UV-NIR Spektrometer
- BRUKER MPA – FT- NIR Spektrometer
- Hamamatsu FT – IR Spektrometer C12606-02
- ARCoptix FT- MIR Rocket 6.0
- Horiba Fluolog FL3-22
- Headwall Photonics VNIR Hyperspectral Imaging System
- SpecIm SP SP-sCMOS-CL50-v10E VIS-NIR Hyperspectral Imaging System
- SpecIm SP-SWIR-CL-400-N25E SWIR Hyperspectral Imaging System
Leistungen der Tierärztlichen Klinik

Die medizinischen Leistungen der Pferdeklinik finden Sie auf der Internetseite der Tierklinik Bad Langensalza.
Die Leistungen der Kleintierpraxis finden Sie auf der Internetseite der der Tierklinik Bad Langensalza hier.